我們圍繞“創新驅動”與“患者可及”,構建了多元化協同互補的產品組合,絕大部分產品均通過自有平臺自主開發,含多個潜在“全球新”靶點藥物,覆蓋惡性腫瘤、自身免疫系統疾病、慢性代謝類疾病、神經系統疾病以及感染性疾病這五大治療領域。
隨著產品管線的不斷豐富和對藥物聯合治療的進一步探索,我們的創新研發領域從單抗藥物擴展至包括小分子藥物、抗體藥物偶聯物(ADCs)、雙特异性或多特异性抗體藥物、融合蛋白、核酸類藥物、疫苗等更多類型的藥物研發以及癌症、自身免疫性疾病的下一代創新療法探索。
產品管線
- 腫瘤
- 自身免疫
- 慢性代謝
- 神經系統
- 感染
- 全球開發
-
JS212
EGFR×HER3 ADC
腫瘤
重组人源化EGFR和HER3双特异性抗体偶联药物(ADC),主要用于晚期恶性实体瘤的治疗
-
JS213
PD-1×IL-2
腫瘤
PD-1和IL-2雙功能性抗體融合蛋白,主要用於晚期惡性腫瘤的治療
-
JS207
PD-1+VEGF
腫瘤
公司自主研發的重組人源化抗PD-1和VEGF雙特異性抗體,主要用於晚期惡性腫瘤的治療
-
JS203
CD3+CD20
腫瘤
公司自主研發的重組人源化抗CD20和CD3雙特異性抗體,主要用於復發難治B細胞非霍奇金淋巴瘤的治療。截至目前,國內尚無同類靶點產品獲批上市
-
JS111
EGFR exon 20
非小細胞肺癌
公司引進的一種有效抑製EGFR非常見突變的靶向小分子抑製劑
-
JS214
VEGF×TGF-β
腫瘤
-
JS110
XPO1
子宫内膜癌
公司與微境生物共同開發的核輸出蛋白XPO1小分子抑製劑
-
JS015
DKK1
腫瘤
公司獨立自主研發的重組人源化抗DKK1單克隆抗體註射液,主要用於晚期惡性實體瘤的治療
-
JS007
CTLA-4
肺癌 黑色素瘤
公司自主研發的重組人源化抗CTLA-4單克隆抗體注射液
-
JT002
小核酸免疫調節劑
季節性過敏性鼻炎
公司與吉盛澳瑪生物共同開發的一款小核酸免疫調節劑,擬用於治療季節性過敏性鼻炎
-
Tifcemalimab
BTLA
肺癌 淋巴瘤等
公司自主研發的全球首個進入臨床開發階段的抗腫瘤抗BTLA單抗。
-
偌考奇拜單抗
IL-17A
銀屑病 脊柱炎
公司自主研發的特异性抗IL-17A單克隆抗體
-
JS001sc
PD-1
腫瘤
公司在特瑞普利單抗基礎上開發的皮下註射製劑
-
JS105
PI3K-α
婦科腫瘤
公司與潤佳醫藥合作開發的靶向PI3K-α的口服小分子抑製劑
-
JS107
Claudin18.2 ADC
消化道腫瘤
自主研發的注射用重組人源化抗Claudin18.2單克隆抗體MMAE偶聯劑
-
特瑞普利單抗
PD-1
腫瘤
公司自主研發、中國首個成功上市的國產抗PD-1單抗; 榮膺國家專利領域最高獎項“中國專利金獎”
-
阿達木單抗
TNF-α
類風濕關節炎等
公司與邁威生物合作開發的阿達木單抗,公司第三款商業化產品
-
氫溴酸氘瑞米德韋片
RdRp
新型冠狀病毒
新型口服核苷類抗SARS-CoV-2藥物,可抑制病毒複製
-
昂戈瑞西單抗
PCSK9
高脂血症
昂戈瑞西單抗公司自主研發、國內首個獲得臨床試驗批件的國產抗PCSK9單克隆抗躰,用於治療原發性高膽固醇血癥和混合型血脂異常
產品詳情
- 商品名:拓益®
- 藥品代號:特瑞普利單抗
- 靶點:PD-1
- 權益:自主研發
特瑞普利單抗注射液(拓益®)作為我國批准上市的首個國產以PD-1為靶點的單抗藥物,獲得國家科技重大專項專案支持,並榮膺國家專利領域最高獎項“中國專利金獎”。
特瑞普利單抗至今已在全球(包括中國、美國、東南亞及歐洲等地)開展了覆蓋超過15個適應症的40多項由公司發起的臨床研究。正在進行或已完成的關鍵註冊臨床研究在多個瘤種範圍內評估特瑞普利單抗的安全性及療效,包括肺癌、鼻咽癌、食管癌、胃癌、膀胱癌、乳腺癌、肝癌、腎癌及皮膚癌等。
截至目前,特瑞普利單抗已在中國內地獲批12項適應症:【1】用於既往接受全身系統治療失敗的不可切除或轉移性黑色素瘤的治療(2018年12月);【2】用於既往接受過二線及以上系統治療失敗的復發/轉移性鼻咽癌患者的治療(2021年2月);【3】用於含鉑化療失敗包括新輔助或輔助化療12個月內進展的局部晚期或轉移性尿路上皮癌的治療(2021年4月);【4】聯合順鉑和吉西他濱用於局部復發或轉移性鼻咽癌患者的一線治療(2021年11月);【5】聯合紫杉醇和順鉑用於不可切除局部晚期/復發或遠處轉移性食管鱗癌患者的一線治療(2022年5月);【6】聯合培美曲塞和鉑類用於表皮生長因數受體(EGFR)基因突變陰性和間變性淋巴瘤激酶(ALK)陰性、不可手術切除的局部晚期或轉移性非鱗狀非小細胞肺癌的一線治療(2022年9月);【7】聯合化療圍手術期治療,繼之本品單藥作為輔助治療,用於可切除IIIA-IIIB期非小細胞肺癌的成人患者(2023年12月);【8】聯合阿昔替尼用於中高危的不可切除或轉移性腎細胞癌患者的一線治療(2024年4月);【9】聯合依託泊苷和鉑類用於廣泛期小細胞肺癌一線治療(2024年6月);【10】聯合注射用紫杉醇(白蛋白結合型)用於經充分驗證的檢測評估PD-L1陽性(CPS≥1)的復發或轉移性三陰性乳腺癌的一線治療(2024年6月);【11】聯合貝伐珠單抗用於不可切除或轉移性肝細胞癌患者的一線治療(2025年3月);【12】用於不可切除或轉移性黑色素瘤的一線治療(2025年4月)。2020年12月,特瑞普利單抗首次通過國家醫保談判,目前12項獲批適應症已全部納入《國家醫保目錄(2025年)》,是目錄中唯一用於黑色素瘤、腎癌、三陰性乳腺癌治療的抗PD-1單抗藥物。特瑞普利單抗用於晚期鼻咽癌和食管鱗癌治療的3項適應症已在中國香港獲批。
在國際化佈局方面,特瑞普利單抗目前已在美國、歐盟、印度、英國、約旦、澳大利亞、新加坡、阿聯酋、科威特、巴基斯坦、加拿大等國家和地區獲得批准上市,並在全球多個國家和地區接受上市審評。
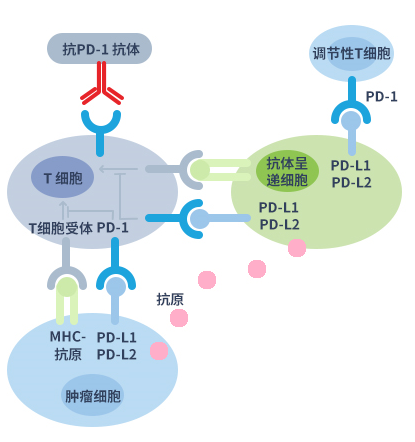
作用机制
PD-1為T細胞表面受體,是T細胞共抑制信號通路的一種免疫檢查點分子。如圖下部分所示,當PD-1與腫瘤細胞表面的配體PD-L1/PD-L2結合,T細胞便接收抑制性信號。通過PD-1與其配體結合致使T細胞免疫失能並因此阻斷抗腫瘤反應。抗PD-1單克隆抗體可阻斷PD-1與PD-L1/PD-L2結合,從而使T細胞的免疫功能恢復。
主要研究文獻
- 序號 期刊名稱 文獻標題 發表時間 链接
- 1 JAMA Oncology Toripalimab vs Dacarbazine as First-Line Therapy for Advanced Melanoma of Acral Subtype: The Phase 3 MELATORCH Randomized Clinical Trial 2026 打開連結
- 2 The Lancet Gastroenterology & Hepatology Toripalimab plus bevacizumab versus sorafenib as first-line treatment for advanced hepatocellular carcinoma (HEPATORCH): a randomised, open-label, phase 3 trial 2025 打開連結
- 3 JAMA Oncology Toripalimab For Extensive-Stage Small Cell Lung Cancer 2024 打開連結
- 4 Journal of the American Medical Association Perioperative Toripalimab Plus Chemotherapy for Patients With Resectable Non-Small Cell Lung Cancer: The Neotorch Randomized Clinical Trial 2024 打開連結
- 5 Nature Medicine Toripalimab plus nab-paclitaxel in metastatic or recurrent triple-negative breast cancer: a randomized phase 3 trial 2024 打開連結
- 6 Journal of the American Medical Association Toripalimab Plus Chemotherapy for Recurrent or Metastatic Nasopharyngeal Carcinoma: The JUPITER-02 Randomized Clinical Trial 2023 打開連結
- 7 Annals of Oncology Toripalimab plus axitinib versus sunitinib as first-line treatment for advanced renal cell carcinoma: RENOTORCH, a randomized, open-label, phase III study 2023 打開連結
- 8 Cancer Cell Toripalimab plus chemotherapy in treatment-naïve, advanced esophageal squamous cell carcinoma (JUPITER-06): A multi-center phase 3 trial 2022 打開連結
- 9 Journal of Clinical Oncology Toripalimab Plus Chemotherapy for Patients With Treatment-Naive Advanced Non–Small-Cell Lung Cancer: A Multicenter Randomized Phase III Trial (CHOICE-01) 2022 打開連結
- 10 Journal for ImmunoTherapy of Cancer Toripalimab plus axitinib in patients with metastatic mucosal melanoma: 3-year survival update and biomarker analysis 2022 打開連結
- 11 Clinical Cancer Research Safety, Efficacy, and Biomarker Analysis of Toripalimab in Patients with Previously Treated Advanced Urothelial Carcinoma: Results from a Multicenter Phase II Trial POLARIS-03 2022 打開連結
- 12 Annals of Oncology Toripalimab (anti-PD-1) versus high-dose interferon-α2b as adjuvant therapy in resected mucosal melanoma: a phase II randomized trial 2022 打開連結
- 13 Nature Medicine Toripalimab or placebo plus chemotherapy as first-line treatment in advanced nasopharyngeal carcinoma: a multicenter randomized phase 3 trial 2021 打開連結
- 14 Signal Transduction and Targeted Therapy Toripalimab plus chemotherapy as second-line treatment in previously EGFRTKIs treated patients with EGFR-mutant advanced NSCLC: a multi-center phase II trial 2021 打開連結
- 15 Journal of Clinical Oncology Efficacy, Safety, and Correlative Biomarkers of Toripalimab in Previously Treated Recurrent or Metastatic Nasopharyngeal Carcinoma: A Phase II Clinical Trial (POLARIS-02) 2021 打開連結
- 16 JAMA Network Open Safety, Antitumor Activity, and Pharmacokinetics of Toripalimab, a Programmed Cell Death 1 Inhibitor, in Patients With Advanced Non–Small Cell Lung Cancer A Phase 1 Trial 2020 打開連結
- 17 Cancer Communications A Phase I Study of Toripalimab, an anti-PD-1 Antibody, in Patients With Refractory Malignant Solid Tumors. 2020 打開連結
- 18 Clinical Cancer Research Safety, Efficacy and Biomarker Analysis of Toripalimab in previously treated advanced melanoma: results of the POLARIS-01 multicenter phase II trial 2020 打開連結
- 19 European Journal of Cancer Safety and clinical efficacy of toripalimab, a PD-1 mAb, in patients with advanced or recurrent malignancies in a phase I study 2020 打開連結
- 20 mABs Glycosylation-independent binding of monoclonal antibody toripalimab to FG loop of PD-1 for tumor immune checkpoint therapy 2019 打開連結
- 21 Acta Pharmacologica Sinica Preclinical evaluation of the efficacy, pharmacokinetics and immunogenicity of JS-001 2017 打開連結
- 22 Clinical Cancer Research Efficacy, safety and biomarkers of toripalimab in patients with recurrent or metastatic neuroendocrine neoplasms:a multiple-center phase Ib trial 2020 打開連結
- 23 Journal of Clinical Oncology Axitinib in Combination With Toripalimab, a Humanized Immunoglobulin G4 Monoclonal Antibody Against Programmed Cell Death-1, in Patients With Metastatic Mucosal Melanoma: An Open-Label Phase IB Trial 2019 打開連結
- 24 Annals of Translational Medicine JS001, an anti-PD-1 mAb for advanced triple negative breast cancer patients after multi-line systemic therapy in a phase I trial 2019 打開連結
- 25 Journal of Hematology & Oncology Safety and clinical activity with an anti-PD-1 antibody JS001 in advanced melanoma or urologic cancer patients 2019 打開連結